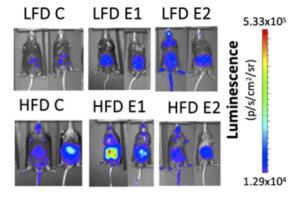
Esta proteína, conocida como S100A4, hasta el momento había sido únicamente investigada como una molécula implicada en el desarrollo de metástasis en muchos tipos de cáncer
Un equipo de científico de la Universidad de Granada (UGR), el Instituto de Nutrición y Tecnología de los Alimentos “José Mataix” del Centro de Investigaciones Biomédicas (CIBM) y el Instituto de Investigación Biosanitaria (ibs.GRANADA) ha demostrado por primera vez que una proteína responsable de la metástasis en muchos tipos de cáncer también provoca alteraciones metabólicas en niños y adolescentes con obesidad.
La proteína, conocida como S100A4, hasta el momento había sido únicamente investigada como una molécula implicada en el desarrollo de metástasis en muchos tipos de tumores. Sin embargo, su alta implicación en procesos moleculares relacionados con la inflamación sistémica la postulaba como una molécula con un papel prometedor para muchas otras patologías más allá del cáncer (entre las que destacan la artritis reumatoide, la esclerosis múltiple o la propia obesidad).
Por primera vez, estos investigadores de la UGR han desvelado la implicación de esta proteína en el desarrollo de importantes alteraciones cardiometabólicas propias de la obesidad infantil, como es el caso de la resistencia a la insulina. Estas alteraciones son las primeras manifestaciones de futuras complicaciones como la aparición de diabetes tipo 2 y enfermedad cardiovascular durante la edad adulta, y suponen una de las principales causas de mortalidad entre la población con obesidad.
Particularmente, el grupo de investigación ha demostrado cómo alteraciones en los niveles sanguíneos de la proteína S100A4 preceden y acompañan el desarrollo de insulinorresistencia en niños con obesidad. Además, han demostrado como los niveles de esta proteína en sangre se elevan de manera exponencial cuando estos niños comienzan su desarrollo puberal y evolucionan hacia la edad adulta, en la que S100A4 se consolida como un robusto marcador biológico asociado con un peor estado metabólico.
 Como novedad, el grupo de investigación de la UGR no solo ha demostrado la asociación entre la elevación sanguínea de esta proteína y la aparición o empeoramiento de la insulinorresistencia propia de la obesidad, sino que además propone alteraciones a nivel genético y epigenético como posibles responsables de su desregulación, ampliando por lo tanto el conocimiento sobre los mecanismos moleculares subyacentes a la aparición de la enfermedad.
Como novedad, el grupo de investigación de la UGR no solo ha demostrado la asociación entre la elevación sanguínea de esta proteína y la aparición o empeoramiento de la insulinorresistencia propia de la obesidad, sino que además propone alteraciones a nivel genético y epigenético como posibles responsables de su desregulación, ampliando por lo tanto el conocimiento sobre los mecanismos moleculares subyacentes a la aparición de la enfermedad.
Los investigadores forman parte de la línea de investigación de las bases moleculares de la obesidad infantil liderada por la Dra. Concepción Aguilera dentro del grupo “BioNit – Bioquímica de la Nutrición e Implicaciones terapéuticas”, del departamento de Bioquímica y Biología Molecular II de la Facultad de Farmacia de la UGR.
El hallazgo ha sido realizado como parte de su trabajo científico desarrollado en el Instituto de Nutrición y Tecnología de los Alimentos “Jose Mataix” del Centro de Investigaciones Biomédicas (CIBM) en el Parque Tecnológico de la Salud de Granada. Además, el grupo forma parte del Instituto de Investigación Biosanitaria(ibs.GRANADA) y de importantes redes científicas tales como la Red “CIBERobn” del Instituto de Salud Carlos III.
Publicado en la revista Metabolism
En el trabajo colaboran otros grupos clínicos de Institutos de Investigación Sanitaria, como el de la Dra. Leis del IDIS de Santiago de Compostela, la Dra. Bueno del IIS de Aragón y la Dra. Gil-Campos del IMIBIC de Córdoba, quienes han permitido reclutar los niños incluidos en el estudio. Para el desarrollo de este trabajo de investigación, el grupo ha contado con fuentes de financiación derivadas de varios proyectos del Fondo de Investigación Sanitaria (FIS) del Instituto de Salud Carlos III.
Los hallazgos presentados han sido recientemente publicados en la prestigiosa revista Metabolism, y desvelan unas funciones que hasta ahora se desconocían en el desarrollo de esta enfermedad.
Este trabajo abre nuevas e importantes vías de trabajo en el campo de la medicina traslacional y personalizada, donde se demandan cada vez más marcadores predictivos que nos permitan anticipar al desarrollo de la enfermedad desde edades muy tempranas y comenzar protocolos de actuación clínica que eviten la aparición de complicaciones futuras.
Particularmente en el caso de la obesidad y las alteraciones metabólicas, la identificación temprana de niños con alto riesgo de complicaciones futuras de insulinorresistencia y/o diabetes tipo 2 es de especial importancia para reducir la mortalidad asociada a la obesidad. Hoy en día, nuevas proteínas como esta S100A4 ofrecen una gran oportunidad para la prevención de enfermedades y podrían ser monitorizadas en sangre como biomarcadores no invasivos entre la población de riesgo. Por otro lado, más allá de las implicaciones diagnósticas, esta investigación ofrece interesantes oportunidades para nuevos enfoques terapéuticos y propone nuevos puntos de encuentro entre la obesidad y el cáncer, una relación que viene estudiándose durante mucho tiempo para la que no se conocen completamente las causas.

 “Ambas hormonas sexuales tienen un papel fundamental en el cáncer de mama, que es el tipo de cáncer más frecuente en mujeres y, actualmente, también la primera causa de muerte por cáncer en la mujer, por encima del cáncer de pulmón”, explica Manuel Picón Ruiz, investigador del departamento de Anatomía y Embriología Humana de la UGR, perteneciente al Centro de Investigación Biomédica (CIBM), al Instituto de Investigación Biosanitaria de Granada (ibs.GRANADA), al Instituto de Biopatología y Medicina Regenerativa (IBIMER) y a la unidad de investigación de excelencia “Modeling Nature (MNat), y coautor de este trabajo.
“Ambas hormonas sexuales tienen un papel fundamental en el cáncer de mama, que es el tipo de cáncer más frecuente en mujeres y, actualmente, también la primera causa de muerte por cáncer en la mujer, por encima del cáncer de pulmón”, explica Manuel Picón Ruiz, investigador del departamento de Anatomía y Embriología Humana de la UGR, perteneciente al Centro de Investigación Biomédica (CIBM), al Instituto de Investigación Biosanitaria de Granada (ibs.GRANADA), al Instituto de Biopatología y Medicina Regenerativa (IBIMER) y a la unidad de investigación de excelencia “Modeling Nature (MNat), y coautor de este trabajo.