Un cumpleaños feliz para Alofisel
Mario Delgado es investigador del Instituto de Parasitología y Biomedicina López Neyra de Granada (CSIC) y actualmente su director científico. Estos días se cumple el aniversario de haber recibido la patente de una investigación que puede mejorar notablemente la calidad de vida de los pacientes con enfermedad de Crohn. Una patente con sello granadino que consolida la marca Granada Salud y pone de manifiesto el alto nivel de los científicos que desarrollan su trabajo en la ciudad en general y en Parque Tecnológico de Ciencias de la Salud en particular.
Pregunta – En primer lugar, enhorabuena.
Respuesta – Muchas Gracias.
P – Ha sido más de una década de estudio y ensayos clínicos que han dado como resultado un medicamento llamado Alofisel.
R – Exacto. El Alofisel es un fármaco destinado a las personas con la enfermedad de Crohn que han desarrollado complicaciones que sólo se pueden resolver mediante la cirugía. Con este medicamento se evita la intervención quirúrgica, mejorando sustancialmente la calidad de vida de los pacientes.
P – ¿Qué tipo de complicaciones?
R – El 28% de los enfermos de Crohn sufren fístulas anales, que les producen infecciones recurrentes con mucho dolor que les genera incontinencia y, en muchos casos, imposibilidad para trabajar. En estos casos la única solución pasa por una operación, que conlleva la incontinencia total y obliga al paciente a llevar una bolsa de defecación permanente. Teniendo en cuenta que la mayoría de los enfermos tienen entre 20 y 35 años de edad, su calidad de vida se reduce considerablemente durante mucho tiempo.
P – ¿Qué acogida ha tenido este medicamento en la comunidad médico-farmacéutica transcurrido ese tiempo?
R – La semana pasada asistí como ponente a un curso organizado en Huelva sobre manejo multidisciplinar de la enfermedad perianal dirigido a los médicos especialistas que tratan esta patología en nuestro país. Ahí tuve consciencia realmente del impacto que había tenido la aparición de este nuevo medicamento en el mercado para la comunidad médica y especialmente la puerta de esperanza que se abría para muchos pacientes que no tenían ninguna otra alternativa terapéutica, salvo la cirugía, en muchos casos devastadora para ellos. La comunidad médica ya no habla de las células madre como una opción de futuro que podría venir a solucionar problemas clínicos ahora sin solución, allí se hablaba de que esta opción ya es el presente. Y por supuesto, como cualquier nueva terapia que llega, especialmente destinada a pacientes muy castigados por la enfermedad, tendremos que ser cautos y esperar a que se confirme la eficacia observada en los ensayos clínicos realizados hasta el momento. La apuesta de Takeda por este medicamento es clara y refleja la confianza que tiene en él. Y por otro lado, recientemente el Ministerio de Sanidad ha aprobado la financiación de Alofisel por parte del sistema nacional de salud. En este punto es importante destacar el esfuerzo que realiza nuestro sistema de salud para financiar este tratamiento, que puede resultar aparentemente bastante caro en principio, y al acuerdo que ha llegado con Takeda bajo un régimen de riesgo compartido, por el que se paga la totalidad del importe del medicamento en caso de éxito del tratamiento en cada paciente. Esto va a hacer posible que los pacientes españoles que lo necesiten se beneficien de un medicamento generado y desarrollado 100% en España.
 P – ¿Cuál ha sido el resultado de su investigación?
P – ¿Cuál ha sido el resultado de su investigación?
R – Hemos descubierto que algunas células madres presentes en el tejido adiposo no sólo tienen capacidad regeneradora (como la que obtenemos de las células madre del cordón umbilical o de médula ósea), sino que pueden regular respuestas autoinmunes e inflamatorias con lo que pueden utilizarse para prevenir, tratar o mejorar enfermedades autoinmunitarias así como trastornos inflamatorios. Esta es la principal novedad de nuestra investigación.
P – Otra de las novedades es el carácter alogénico de estas células
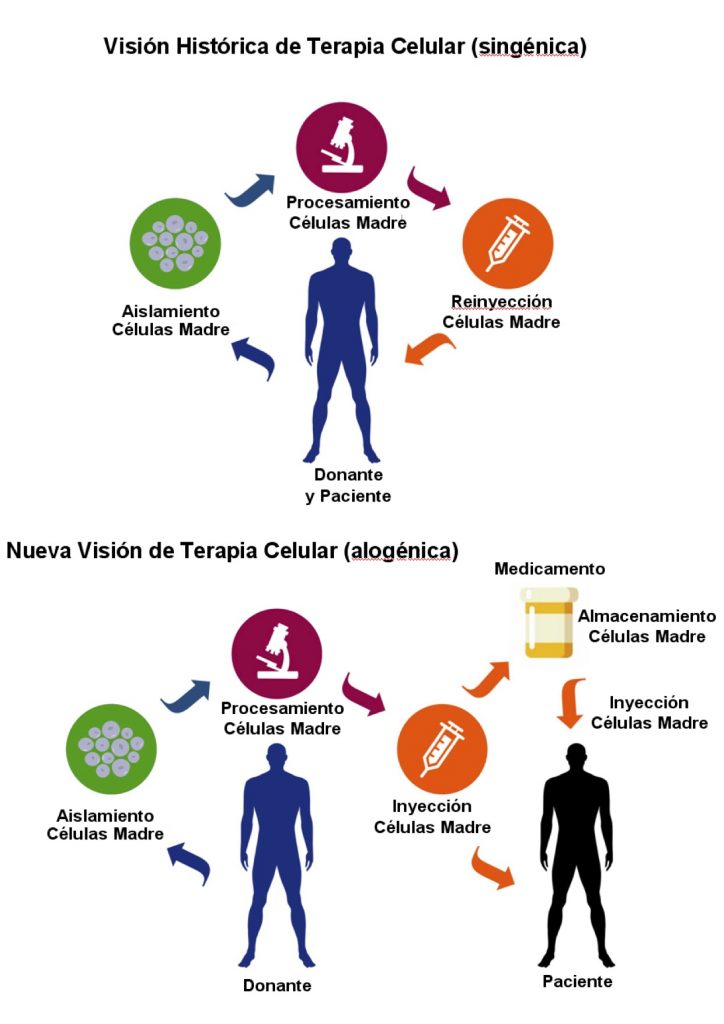
R – Cierto. Hasta hace poco toda la terapia celular estaba basada en un escenario singénico, esto quiere decir que las células madre sólo se utilizaban para la regeneración celular de tejidos del mismo paciente. Sin embargo a veces el paciente no tiene células suficientes o no hay tiempo de expandidlas adecuadamente. Lo que hemos conseguido es trabajar en un escenario alogénico, donde enfermo recibe las células de un donante que una empresa farmacéutica puede expandir, guardar y enviar a cualquier lugar del mundo para que pueda infundirlas cualquier equipo médico. Es como inyectarse cualquier antiinflamatorio con la ventaja de que no hay ningún riesgo de rechazo. Fíjate hasta que punto esto es así, que en nuestra investigación transplantamos células de humanos a ratones y no hubo ningún tipo de reacción inmunológica a las nuevas células. Por eso tienen una aplicación tan amplia. Son, además, muy seguras y no tendrán tumores tras mas de ocho años de seguimiento.
P – ¿Cualquier persona puede, entonces, ser donante?
R – Si, cualquier persona puede donar y recibir. Hay que tener en cuenta que para este tratamiento utilizamos el tejido adiposo que todos tenemos en la zona abdominal y que habitualmente se extrae en las liposucciones estéticas. Esta grasa es la principal fuente de células madre del cuerpo, en mayor medida que las que hay en el cordón umbilical y en la médula ósea. La idea es reutilizarla, ya que ahora se desecha en los hospitales, para conseguir células, aislarlas, expandirlas y guardarlas en nitrógeno listas para su distribución. No se necesita un registro de donantes ya que de cualquier liposucción se consiguen células. Incluso hay hospitales que costean el tratamiento a cambio de poder utilizar la el tejido adiposo extraído del donante.
P – ¿Cómo han ido los ensayos clínicos que se exigen para lanzar un medicamento?
R – En marzo de 2018, la agencia europea del medicamento (EMA) autorizó la comercialización de Alofisel en toda Europa, convirtiéndose en el primer medicamento basado en terapia celular de donante para el tratamiento de cualquier enfermedad. Esto solo ocurre no sólo habiendo pasado el medicamento por todas las fases clínicas de seguridad y eficacia (fase I, II y III), sino que la EMA después de analizar los resultados derivados de estos ensayos considera que la eficacia y seguridad del medicamento, junto con la necesidad clínica de este tipo de tratamiento, son suficientemente elevados como para recomendar y autorizar su venta en Europa.
P – ¿En cuántos países puede hallarse el medicamento?
R – Hasta el momento Alofisel se comercializa en 13 países europeos, entre ellos Alemania, Austria, Holanda, Finlandia, Israel y Suiza. España ha sido el último en sumarse a la lista de países cuyo sistema nacional de salud financiará Alofisel para su uso en los pacientes con enfermedad de Crohn que necesiten el tratamiento de fístulas complejas anales y que no respondan a los tratamientos actuales.
P – Las células madre que se usan para este medicamento salen de liposucciones. ¿Habrá suficientes donaciones de este tipo para su producción?
R – Estamos hablando de que este medicamento lo va a comercializar una de las empresas biofarmacéuticas Top10 del mundo, y la más importante en el campo de la gastroenterología. Takeda ha pagado 540 millones de euros por la compra de esta tecnología en exclusividad, y acaba de invertir otros 10 millones en la planta de producción de este medicamento en Tres Cantos (Madrid) para duplicar su producción y asegurar el suministro de Alofisel a cualquier lugar del territorio europeo. El hecho que se puedan usar estas células de forma alogénica, por otro lado uno de nuestros principales avances, ha hecho que una terapia celular que se podía aplicar de forma ocasional se convierta en un medicamento, que se producirá en Madrid y se distribuirá a cualquier hospital o clínica de Europa en menos de 48 horas. La mayoría de las células madre que forman Alofisel provienen de liposucciones de personas sometidas a cirugía estética, y para esto, créeme, hay muchos/as donantes voluntarios/as en España. Además no te puedes imaginar la cantidad de células madre que podemos sacar de estas liposucciones, especialmente después de someterlas a un proceso de expansión previo al almacenaje y/o envío.
P – Por este descubrimiento ha recibido el Premio Galeno en la categoría de terapias avanzadas.
R – Si, y estamos muy satisfechos ya que este premio está considerado como el Nobel de la industria farmacéutica. Han sido cinco años de investigación y otros trece de ensayo clínico que, al final, ha tenido su recompensa.
 P – ¿Hablamos de una solución definitiva?
P – ¿Hablamos de una solución definitiva?
R – En el 55% de los pacientes, si. Es una cifra bastante buena teniendo en cuenta que el medicamento se está suministrando a pacientes en los que han fallado todos los tratamientos anteriores y encuentran médicamente deshauciado. Cuando se demuestre su eficacia probablemente se convierta en primera línea de tratamiento.
P – Y, ¿estará al alcance de todos los pacientes?
R – Si me preguntas por el precio, es algo complicado, porque la compañía que los comercializa negocia su coste con cada país. Lo que en España cuesta, por ejemplo, 10 euros, en Francia puede costar 5. Es cierto que por ahora no es un medicamento barato. Hablamos de entre 60.000 y 120.000 euros, aunque la empresa podría rebajarlo a 30.000 en algunos países. Todo depende del número de pacientes que lo necesiten.
P – ¿De cuántos pacientes estaríamos hablando?
R – El problema con la enfermedad de Crohn es que no existe un censo de enfermos, sólo tenemos estimaciones. Se calcula que hay en España unos 140.000 afectados, de los cuales el 28% presentan fístulas anales completas y de ellos, al 5% les fallan todos los tratamientos existentes hasta ahora. Estaríamos hablando de unos 80.000 pacientes en Europa.
P – ¿ALOFISEL va a desplazar a otros tratamientos médicos?
R – No. En este momento, Alofisel está únicamente indicado en aquellos enfermos de Crohn con fístulas perianales complejas (en opinión de los propios enfermos, la peor manifestación de esta enfermedad que pueden sufrir) que no han respondido a los tratamientos que tenemos actualmente en clínica, y cuya única alternativa será básicamente someterse a multitud de cirugías, que en la mayoría de los casos termina con un estoma intestinal e incontinencia de por vida. Por lo tanto, no podemos hablar actualmente de desplazar a otros tratamientos, sino de dar solución u ofrecer una oportunidad terapéutica a aquellos pacientes que no responden al tratamiento actual. En un futuro, si se demuestra la eficacia a largo plazo que se ha observado en los ensayos clínicos realizados hasta el momento, se plantearía la posibilidad de empezar el tratamiento en pacientes en un estado anterior, y no esperar a que fallen a los tratamientos actuales, y en ese caso, si podríamos hablar de desplazar al menos a la terapia con anti-TNF que es la que actualmente se impone, pero que está fallando en muchos pacientes desde el primer momento. Por otro lado, la actividad anti-inflamatoria e inmunosupresora que descubrimos en estas células, abre un abanico de tratamientos futuros para otras patologías donde la respuesta inmunológica está alterada.
P – Sería muy interesante si este tratamiento se pudiera aplicar a otras enfermedades
R – Sí que se puede, por ejemplo en la artritis reumatoide. Hay un ensayo clínico para el tratamiento de pacientes en los que, igual que con la enfermedad de Crohn, han fallado otros medicamentos. Hay otro ensayo patentado por la investigadora Elena González Rey sobre su aplicación en pacientes con septicemia originada por una neumonía hospitalaria, que causa muerte en el 30% de los casos. Ya no sólo hablamos de pacientes, sino de la propia vida. Los primeros datos son muy prometedores pero dependemos de que las farmacéuticas apuesten por ellos.
P – Por último, desde tu experiencia, ¿cómo se vive personalmente un descubrimiento de este tipo, qué dudas asaltan? ¿cómo se puede cuantificar en tiempo, medios y demás el trabajo realizado?
R – La mayoría de los investigadores vivimos nuestro trabajo con pasión. Nos emocionamos cuando conseguimos cambiar la expresión de un gen alterado, aún más cuando conseguimos cambiar la función alterada de una célula, y todavía más cuando conseguimos reducir los síntomas de una enfermedad en un animal de experimentación. Teniendo en cuenta esto (que puede ocurrir varias veces en nuestra vida), no te puedes imaginar lo que uno puede sentir que su trabajo de tantos años ha resultado en un medicamento que está curando a personas de todo el mundo. La sensación de que tu esfuerzo va a ayudar a tanta gente, en principio desahuciada clínicamente, gente que no conoces, es indescriptible. Es cerrar el círculo. Ahora bien, no te vayas a pensar que esto es fácil. Es más, casi nunca ocurre. De hecho, en estos días en la prensa se está presentando el desarrollo de este medicamento innovador como un hito de la ciencia española y un ejemplo de colaboración publico-privada. Y no debemos olvidar, que toda investigación traslacional, incluida esta, parte de una investigación básica sólida. Y no nos equivoquemos, para que haya resultados de este tipo que llegue a los pacientes, tiene que fortalecerse la inversión en investigación básica. El desarrollo de Alofisel ha llevado más de 15 años, el esfuerzo conjunto de un grupo de investigación como el nuestro, un equipo médico liderado por el Dr. Damián Garcia Olmo y la apuesta desde el principio de la industria farmacéutica, inicialmente con Cellerix-Tigenix y finalmente con Takeda, por una estrategia terapéutica que ha cambiado y va a seguir cambiando el campo de la terapia celular. Este es el mejor ejemplo de cuando se hacen las cosas bien en ciencia e innovación desde el principio, con perseverancia y sin perder el foco de que lo importante es el paciente, se puede conseguir generar un medicamento innovador, incluso desde España.
P – Estamos ante un nuevo logro de la marca Granada Salud.
R – Efectivamentey es importante que se reconozca y se divulgue. Es necesario lanzar la idea de que si no hay colaboración entre las diferentes instituciones no es posible que se puedan desarrollar estos avances científicos El germen es granada, es importante lanzar la ide de que si no colaboran con otra instituciones es imposible que se puedan desarrollar estos avance científicos.






 P – ¿Cuál ha sido el resultado de su investigación?
P – ¿Cuál ha sido el resultado de su investigación? P – ¿Hablamos de una solución definitiva?
P – ¿Hablamos de una solución definitiva?